根据国家药品监督管理局最新公示显示,复星凯特CAR-T细胞治疗产品益基利仑赛注射液(又称阿基仑赛,代号:FKC876)获得批准上市。

这意味着中国终于迎来了首款CAR-T疗法上市,这也是中国首款获批上市的CAR-T细胞治疗产品,相信紧随其后,中国将全面进入CAR-T细胞疗法新时代。
什么是CAR-T疗法?
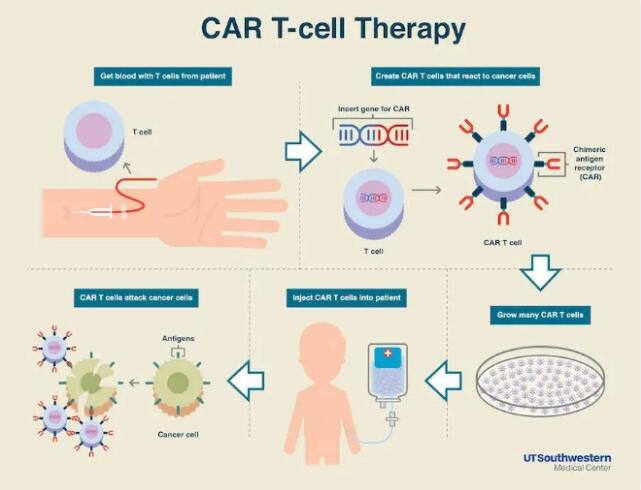
CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy)免疫细胞治疗是通过基因工程修饰患者自体T细胞,以表达靶向肿瘤抗原的嵌合抗原受体分子,由激活的T细胞介导杀伤肿瘤细胞。
2020年7月??获批的吉利德/Kite的CAR-T疗法Tecartus,用于治疗复发/难治性套细胞淋巴瘤(MCL)成人患者,这是首款获批治疗MCL的CAR-T疗法;
2021年3月??获批的百时美施贵宝/Bluebird共同研发的CAR-T疗法Abecma,用于治疗经过4种或更多种先前疗法(包括免疫调节剂,蛋白酶体抑制剂和抗CD38单克隆抗体)的复发/难治性多发性骨髓瘤患者。这是首个获FDA批准上市的靶向BCMA的CAR-T疗法。
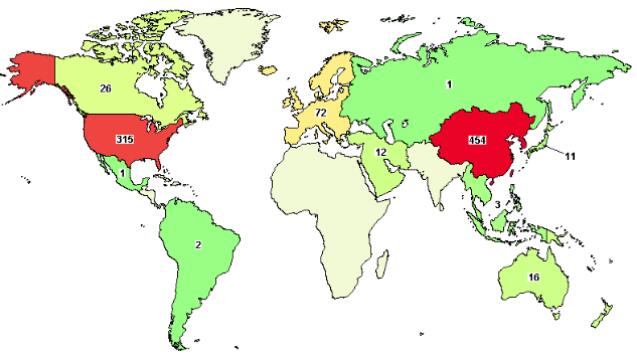 根据世界临床试验中心的数据,目前中国和美国已经成为全球最大的CAR-T细胞疗法的研发国,临床试验项目远高于其他国家。在国内,已有335个正在进行的CAR-T临床试验,其中,多款产品即将步入商业化阶段。且在前期扎堆于CD19靶点之后,国内很多CAR-T细胞疗法已经将眼光瞄准实体瘤,寻找使用CAR-T细胞疗法突破实体瘤治疗的契机。
根据世界临床试验中心的数据,目前中国和美国已经成为全球最大的CAR-T细胞疗法的研发国,临床试验项目远高于其他国家。在国内,已有335个正在进行的CAR-T临床试验,其中,多款产品即将步入商业化阶段。且在前期扎堆于CD19靶点之后,国内很多CAR-T细胞疗法已经将眼光瞄准实体瘤,寻找使用CAR-T细胞疗法突破实体瘤治疗的契机。
公司CAR-T细胞疗法科研进展

声明:本文部分图文来源于互联网,如有侵权请联系小编撤稿。
 关注官方微信
关注官方微信
-3.png)




